La malattia di Alzheimer Perusini (Alzheimer Disease, AD) è la forma più frequente di demenza, colpisce infatti circa 17 milioni di persone nel mondo. I sintomi più frequenti sono la difficoltà nel ricordare eventi recenti, afasia, disorientamento, cambiamenti repentini di umore, depressione, incapacità di prendersi cura di sé, problemi nel comportamento. Attualmente nonostante l’assenza di una cura effettiva e la variabilità della velocità di progressione, l’aspettativa media di vita dopo la diagnosi è dai tre ai nove anni, grazie alla somministrazione di trattamenti terapeutici con benefici sintomatici.
L’encefalo nell’AD si presenta ridotto di peso e volume, con una marcata e diffusa atrofia che coinvolge tuti i lobi, con maggiore incidenza in quello temporale, nell’ippocampo e nella regione ippocampale. Gli elementi istopatologici caratteristici dell’AD sono le degenerazioni neurofibrillari, l’angiopatia amiloidea e le placche senili.
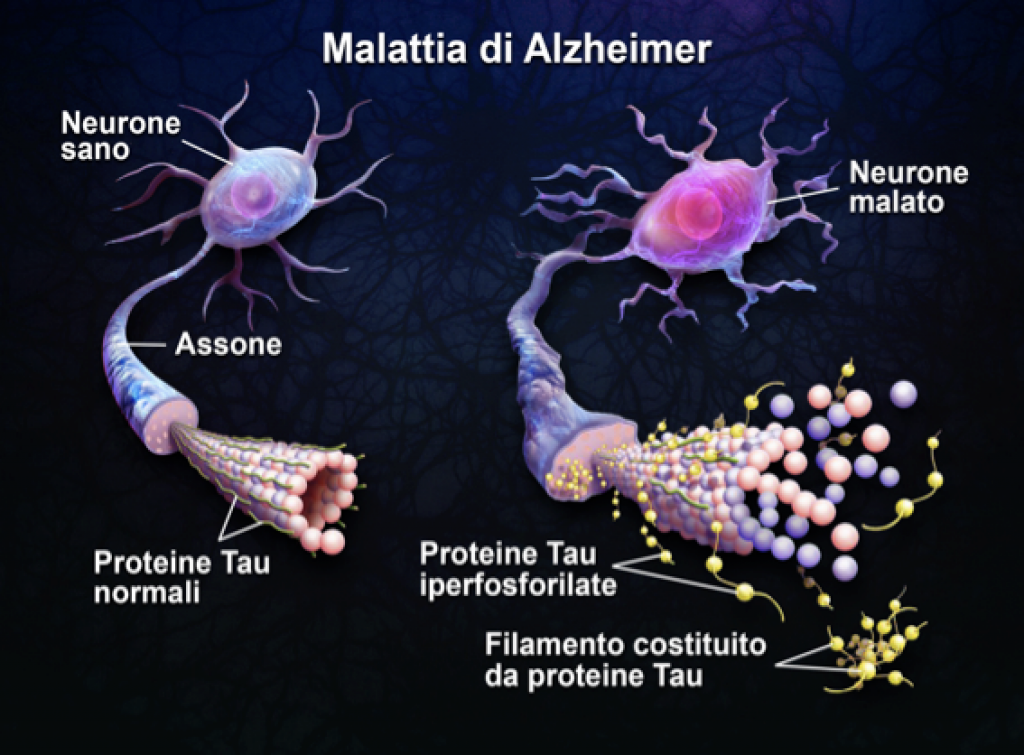
Le degenerazioni neurofibrillari sono costituite da anomali fasci compatti di filamenti chiamati “filamenti elicoidali appaiati” costituiti dalla proteina Tau che, quando viene iperfosforilata, ne causa l’accumulo. La patologia della proteina Tau interverrebbe secondariamente e da sola non sarebbe sufficiente a causare la patologia.
L’angiopatia amiloidea è determinata dal deposito di beta-amiloide nelle pareti delle arteriole cerebrali e leptomeningee.
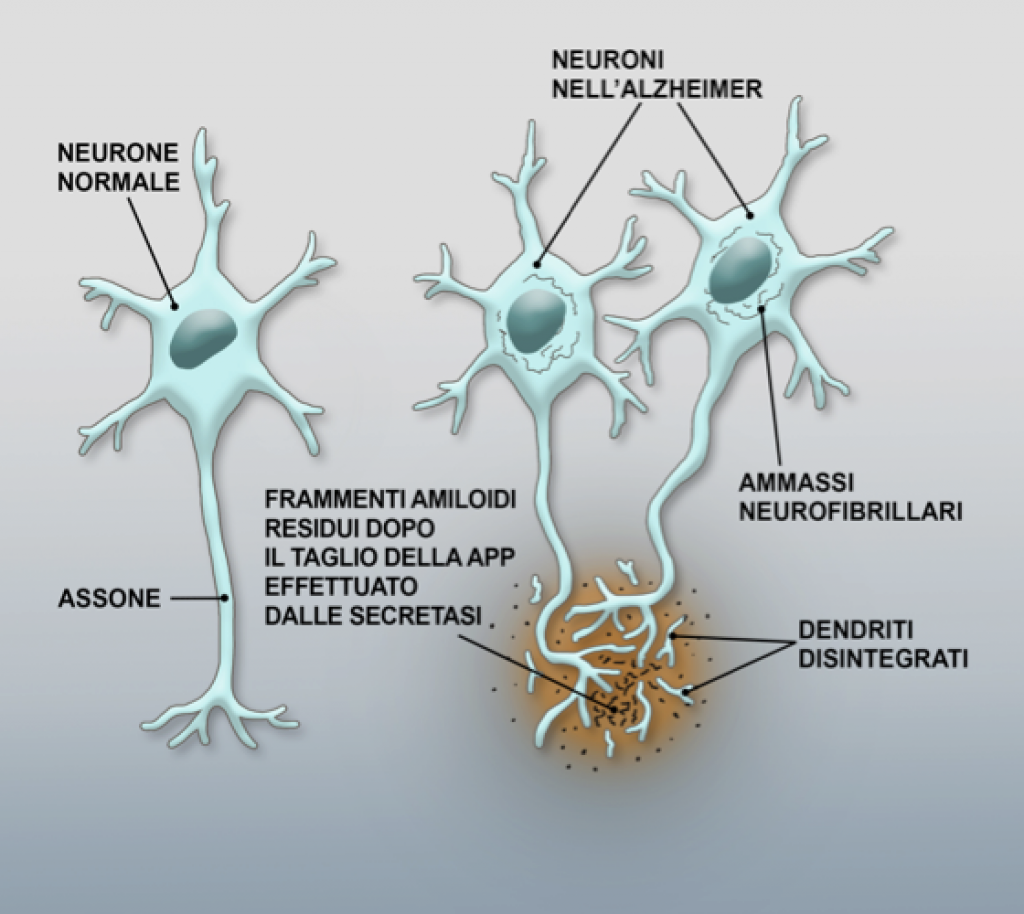
Le placche senili sono determinate da una mutazione della APP (Amyloid Precursor Protein, Proteina Precursore dell’Amiloide), che può aumentare la quantità totale di β-amiloide. La degradazione della APP prodotta avviene sulla superficie cellulare e vede coinvolti tre enzimi che operano tagli proteolitici: la α-secretasi, la β-secretasi e la γ-secretasi. La β-secretasi e la γ-secretasi portano alla produzione di due peptidi di 40 e 42 amminoacidi, chiamati beta-amiloide (Aβ40 e Aβ42). Il secondo peptide (Aβ42) è considerato il più tossico a livello neuronale. Nei soggetti sani la α-secretasi è l’enzima principalmente deputato al processo di degradazione della APP, mentre si ipotizza che nei soggetti malati l’enzima che interviene sulla APP sia la β-secretasi, con una larga produzione di proteina beta-amiloide. La degenerazione dei neuroni potrebbe verosimilmente essere la conseguenza di una neuro-tossicità legata ai depositi di β-amiloide e a una diminuzione dell’acetilcolina, che porterebbe all’impossibilità per il neurone di trasmettere gli impulsi nervosi e quindi alla morte del neurone stesso, con conseguente atrofia progressiva del cervello.
Oltre che a livello encefalico, l’AD colpisce anche gli occhi. La retina dei pazienti malati di Alzheimer presenta infatti tratti patologici quali l’assottigliamento dello strato delle fibre nervose, la degenerazione delle cellule ganglionari retiniche, riduzione del flusso sanguigno, alterazioni vascolari, presenza di depositi di β-amiloide e di proteina Tau iperfosforilata. La presenza delle placche è facilitata dal trasporto vescicolare della proteina precursore dell’amiloide attraverso gli assoni del nervo ottico che connettono la retina al cervello. Le analisi con il microscopio elettronico e il Congo Red (un composto organico con qualità di birifrangenza, verde-mela, sotto luce polarizzata) hanno confermato la presenza di tale placche.
La malattia di Alzheimer è di solito diagnosticata clinicamente dalla storia del paziente, da osservazioni cliniche, dalla presenza di particolari caratteristiche neurologiche e neuropsicologiche e per l’assenza di condizioni alternative. Quindi generalmente si procede per esclusione, accertando l’assenza di altre malattie dopo un attento esame delle condizioni fisiche e mentali, che viene effettuato con tecniche di Neuroimaging quali EEG, TAC, RM, PET e SPECT che, oltre ad essere molto costose, sottopongono il paziente a isotopi radioattivi.
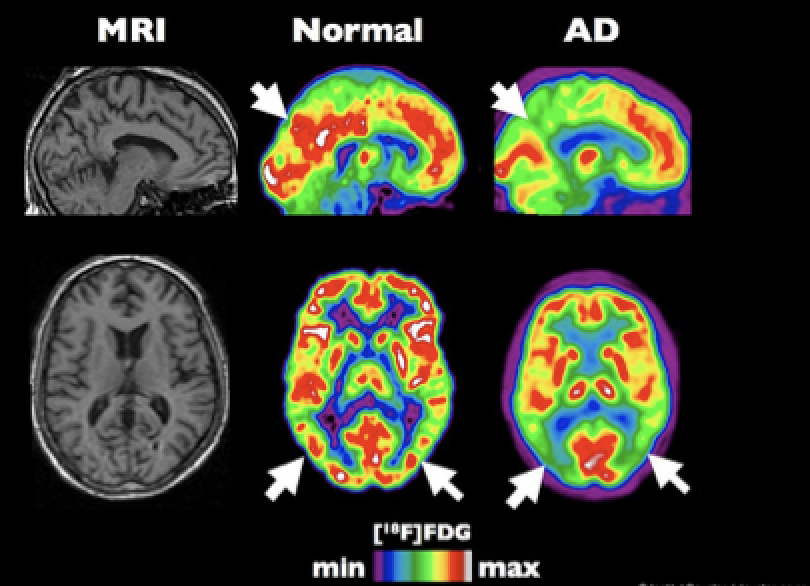
Per tali motivi è stato sviluppato un nuovo metodo non invasivo di imaging delle placche amiloidee retiniche con un OCT, che sfrutta l’autofluorescenza della curcumina lipidica solida, un naturale fluorocromo che lega le fibrille di β-amiloide. Questo metodo permette la valutazione del peso e della distribuzione geometrica delle placche nella retina grazie alle immagini fluorescenti delle placche di beta-amiloide positive alla curcumina. Somministrando ai pazienti curcumina solida per una durata di trenta giorni, si evidenzia un aumento dell’intensità della fluorescenza nel primo e nel decimo giorno, mentre già al ventinovesimo si evidenzia un decadimento.
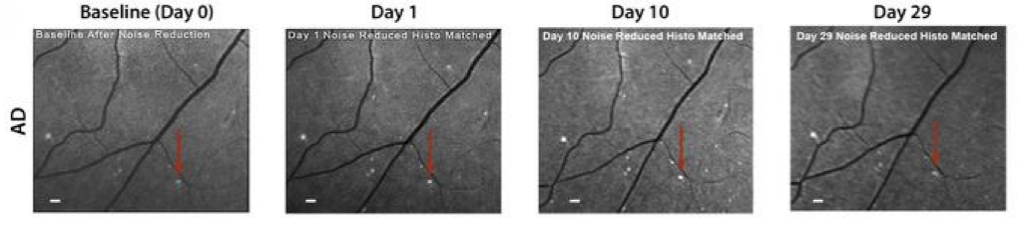
Le immagini ottenute tramite OCT mostrano placche di beta-amiloide similari per morfologia a quelle cerebrali, con dimensioni di 6-7 volte più piccole, all’interno dei vasi sanguigni e lungo le loro pareti, localizzate principalmente nello strato delle cellule ganglionari e sopra la membrana limitante esterna. Il numero di placche maggiore e con area più estesa si riscontra nella media-lontana periferia del quadrante temporale-superiore e temporale-inferiore della retina.
Una marcata perdita di cellule nello strato delle fibre nervose, nello strato nucleare interno e nello strato nucleare esterno si pone in contrasto con l’epitelio pigmentato retinico (EPR) e la membrana di Bruch intatti, evidenziando la presenza di placche sopra l’EPR. È possibile che le differenze nel flusso sanguigno retinico, il diametro dei vasi, lo spessore coroideale, la permeabilità tissutale e la stimolazione luminosa siano alcuni dei fattori che influenzano la velocità (o l’assenza) di deposito della beta-amiloide. Alla luce dei risultati è stato sviluppato un punteggio dell’indice dell’amiloide retinica (RAI, Retinal Amyloid Index) classificando i depositi in base a numero, area, intensità e distribuzione, in questo modo i pazienti con AD presentano valori tra 55.7 e 65.
In base alle immagini ottenute durante lo studio per lo sviluppo di questa nuova tecnica, è stato dimostrato come l’accumulo di depositi a livello retinico sia un antefatto nella patogenesi dell’Alzheimer. Di conseguenza sembra sia possibile aggiungere questa metodica diagnostica a quelle già esistenti per lo screening della popolazione a rischio, la diagnosi e il monitoraggio per la risposta alla terapia. Il fatto che i depositi di amiloide riscontrabili a livello retinico costituiscano un elemento precoce nello sviluppo della malattia fa immaginare che questo dato clinico-strumentale rappresenterà nel prossimo futuro un elemento fondamentale per poter effettuare una diagnosi precoce e ricorrere in modo tempestivo a una terapia mirata e adeguata.
Reference:
Yosef Koronyo et al. (August 17, 2017) ‘’Retinal amyloid pathology and proof-of-concept imaging trial in Alzheimer’s disease’’. JCI insight. 2(16):e93621. https://doi.org/10.1172/jci.insight.93621